土壤污染类型复杂,重金属、石油烃、持久性有机污染物、有机卤化物等大量生产排放并最终进入土壤,使土壤构成、结构、功能发生变化,形成严重的土壤环境污染,危及人体和生态健康.最新《全国土壤污染状况调查公告》显示,重金属镉(Cd)污染点位超标率达7%,大量的土壤调查研究也显示Cd污染在各类重金属中尤为严重,污染率高,污染指数大[1].土壤中Cd过量存在时,会对大部分生物机体产生毒害作用,影响动植物的生长,且Cd在动植物中的累积作用会使之进入食物链,危害人体健康.同时Cd也会危害土壤微生物群落结构和组成,影响土壤酶活性,改变土壤质量[2].由于Cd污染问题突出,有关Cd污染土壤的风险评估和修复研究也得到广泛关注,土壤Cd的形态和生物有效性是决定其风险和修复的重要因素.
柠檬酸作为天然低分子量有机酸,其结构被认为是一种螯合剂,对土壤Cd形态会产生影响并促进其释放,进而提高植物吸收和积累土壤中的Cd[3],这一方面可能增加了Cd的生态风险,但同时对土壤植物修复来说,又是一种非常适合的强化剂.柠檬酸之类的小分子有机酸一方面与重金属发生络合、酸化和还原反应,将重金属溶解释放出来[4],另一方面土壤不同成分也会吸附有机酸,增加土壤表面官能团,为重金属提供更多的吸附位点,促进重金属的吸附,有些重金属还能与有机酸形成土壤⁃络合剂⁃重金属复合体被固定在土壤中,降低重金属的迁移[5].Liu et al[6]报道了添加柠檬酸能够有效提高东南景天地上部对重金属Cd和Pb的吸收富集.Ehsan et al[7]研究表明施加外源柠檬酸不仅可以增加欧洲油菜对Cd的吸收还能缓解Cd对欧洲油菜的胁迫,有利于促进植物对Cd的富集修复.尽管目前的研究倾向于认为柠檬酸的增加对土壤Cd起活化促进吸收的作用,但王学锋等[8]研究表明,柠檬酸施加一周后,四川黄芥地上部对Cd的吸收并没有明显改善.说明土壤性质,污染物实际状况以及植物的种类都有可能影响Cd的环境行为.
本研究通过温室盆栽实验,进行不同的土壤污染类型—重金属Cd单一和复合(与典型多环芳烃芘)污染处理,选择常见的修复树种金丝垂柳(Salix×aureo⁃pendulaCL 'J1011'),通过分析柳树对土壤中Cd和芘的吸收富集,柳树光合作用、生物量和矿质元素差异,了解柠檬酸对土壤中Cd和芘环境行为的影响,评估柠檬酸强化柳树植物修复Cd和芘污染的可行性.
1 材料与方法
1.1 实验材料
供试柳树为金丝垂柳1011(Salix×aureo⁃pendula CL 'J1011'),购自江苏省林业科学研究院.供试土壤采自中国江苏省南京市江宁区野外实验小区(118.96°E,32.12°N)老化十年的Cd污染土壤,分别取Cd污染和空白对照(0~20 cm)表层土.土壤pH 8.02,阳离子交换量43.20 mol·kg-1,总碳含量1.54%,有机质26.61 mg·kg-1,总氮0.11%,总磷0.44 g·kg-1,总钾14.28 g·kg-1,速效磷3.78 mg·kg-1,速效钾145.33 mg·kg-1,碱解氮107.17 mg·kg-1.
1.2 实验设计
表1 各实验处理组污染物浓度
Table 1
| 处理组 | CK | PYR | Cd | Cd⁃PYR |
|---|---|---|---|---|
| Cd (mg·kg-1) | 0.58±0.03 | 0.59±0.02 | 5.40±0.18 | 5.21±0.08 |
| PYR (mg·kg-1) | not detected | 15.72±0.87 | not detected | 15.20±0.71 |
1.3 样品采集
60 d后分别收取柳树根、木质部、韧皮部和叶,并采集根际土壤样品.植物样品洗净后用无尘纸擦拭干净,称量鲜重,经冷冻干燥后计干重,粉碎过筛后放入-80 ℃冰箱冷冻待分析.充分混匀每个处理组中的土壤样品,并将其分成两份,一份自然风干后研磨过筛待分析,一份冷冻干燥后研磨过筛并放入-80 ℃冰箱待分析.
1.4 分析方法
样品中Cd含量:取0.3 g土壤样品或0.5 g植物样品,分别用HNO3⁃HClO4⁃HF和HNO3⁃HClO4消解,超纯水定容,火焰原子吸收分光光度法(THEMO M6 AAS)和电感耦合等离子体发射光谱仪(ICP⁃AES,Perkin Elmer Optima 8000,Waltham,MA,USA)进行测定.
样品中PYR含量:2 g土壤样品或1 g植物样品,参照袁馨等[10]的方法进行前处理,HPLC/UV测定条件:流动相为甲醇∶水(v∶v=87∶13),进样量20 µL,流速1.0 mL·min-1,柱温30 ℃,235 nm波长处检测.检测限为54.9 pg·L-1.植物样品的加标回收率为85.18% (n=5,RSD<7.6%);土壤样品的加标回收率为91.43% (n=5,RSD<5.5%).
植物叶片光合色素:0.25 g鲜叶,破碎后加5 mL无水乙醇与80%丙酮(v∶v=1∶1)混合浸提液,室温黑暗浸提48 h,乙醇稀释后,在663,645,470 nm波长下测定光密度值,计算柳树叶片中叶绿素a、叶绿素b、类胡萝卜素的含量.计算公式如下:
其中,Ca,Cb,Cxc分别代表叶绿素a,b和类胡萝卜素的浓度,A663,A645,A470分别代表波长663,645,470 nm下的吸光度值.P为光合色素含量(mg·g-1),C为色素浓度(g·L-1),V为提取液体积(L),n为稀释倍数,w为叶片鲜重(g).
气体交换参数:采集样品前,选取从柳树顶端往下第三个成熟叶片,采用Li⁃6800便携式光合仪(Li⁃6800,LiCor Inc. Lincoln,Nebraska,USA),测定净光合速率(Pn)、细胞间CO2浓度(Ci)、气孔导度(gs)等气体交换参数.光合测定系统叶室内光照强度设定1000 μmol·m-2·s-1,CO2浓度400 µmol·mol-1,温度为25 ℃.
叶绿素荧光参数:同上采用Li⁃6800便携式光合仪测定叶片8000 μmol·m-2·s-1光强下稳态荧光(Fs)、最大荧光(Fm′)和最小荧光(Fo′),将叶片暗适应30 min,测定柳树叶片的初始荧光(Fo)和最大荧光(Fm).根据测定的荧光参数计算PSⅡ最大光化学效率
植物营养元素:0.5 g植物样品HNO3⁃HClO4消解,超纯水定容过膜,用电感耦合等离子体发射光谱仪(ICP⁃OES)进行测定.
土壤重金属有效态:采用DTPA浸提法,称取过1 mm筛的土壤风干样品5.0 g,加DTPA(diethylenetriaminepentaacetic acid)提取剂10.0 mL,于25 ℃,180 r·min-1振荡2 h后取上清液,火焰原子吸收分光光度法(THEMO M6 AAS)测定Cd浓度.
1.5 数据处理
植物重金属Cd的生物富集系数(bioconcentration factor,BCF)和转运系数(translocation factor,TF)的计算公式如下:
其中,Cwillow为柳树组织Cd含量(mg·kg-1 DW).Csoil为根际土Cd含量(mg·kg-1 DW),Croot为根部Cd浓度(mg·kg-1 DW),Cshoot为地上部Cd浓度(mg·kg-1 DW).
数据处理采用Origin 2018作图,SPSS 20.0进行显著性分析,单因素方差分析(one⁃way ANOVA)进行比较分析.实验结果表示为平均值±标准差(n=4),p<0.05表示差异显著.
2 实验结果与讨论
2.1 柠檬酸对柳树富集Cd和PYR的影响
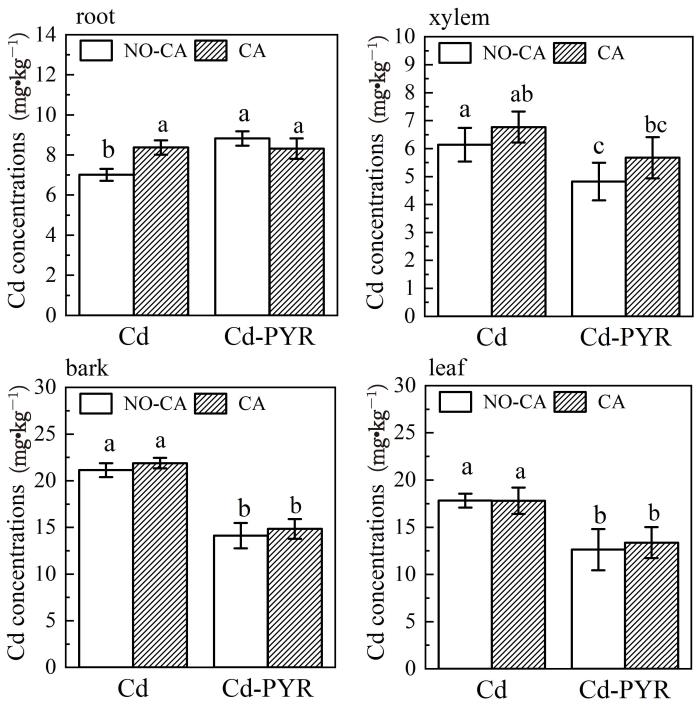
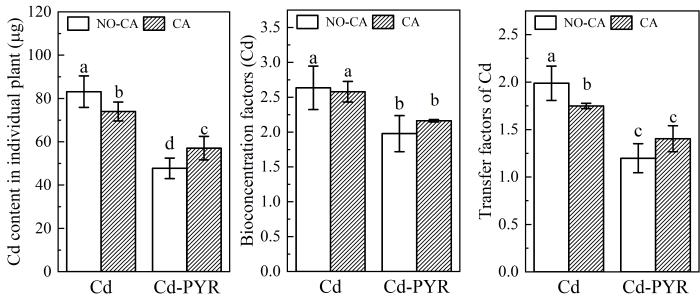
由图1可知,Cd在柳树不同组织的含量为叶>韧皮部>根>木质部.在单一Cd污染土壤中,添加柠檬酸未影响柳树地上部组织(木质部、皮部和叶)中的Cd浓度,但显著增加了柳树根部的Cd富集(p<0.05);在Cd⁃PYR复合污染土壤中,柠檬酸对柳树各部分组织中Cd浓度均未产生显著影响.与单一Cd污染相比,Cd⁃PYR复合污染增加了柳树根部的Cd浓度,但抑制了其地上部组织中Cd浓度(p<0.05),这可能是PYR的存在影响了柳树对重金属的转运能力.图2进一步分析柠檬酸对柳树富集Cd的影响,发现在单一Cd污染处理组中,柠檬酸显著降低了柳树对Cd的提取总量和转运系数(TF),抑制率分别为11.0%和12.0%;在Cd⁃PYR复合污染组中,添加柠檬酸显著提高了柳树对Cd的提取总量(19.5%).
图1
图1
Cd在柳树不同组织中的浓度
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.1
Cd concentrations in plant tissues of willow at different treatments
图2
图2
柠檬酸对柳树提取和转运Cd的影响
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.2
Effects of citric acid on Cd phytoextraction by willow
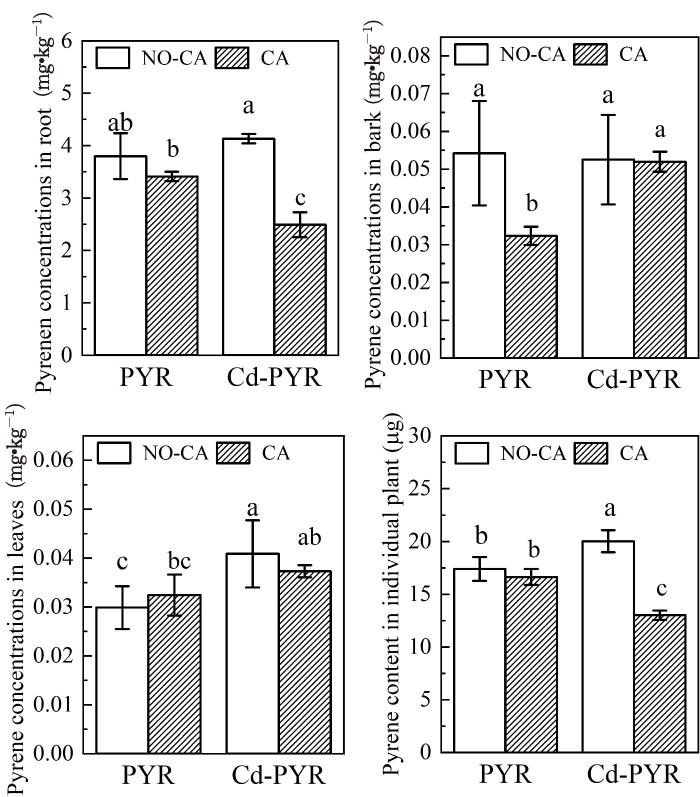
由图3可知,柳树对PYR的吸收主要在根部,皮与叶片中PYR含量较少,木质部中未检测到PYR的存在.添加柠檬酸减少了柳树根部对PYR的吸收,在Cd⁃PYR复合污染下,柠檬酸使根部PYR浓度显著减少了39.7%,而在单一PYR污染下则略有减少.种植60 d后,每棵柳树对PYR的吸收总量为13.0~20.0 μg,在Cd⁃PYR复合污染中,添加柠檬酸使柳树对PYR的吸收总量减少了35.0%.PYR在土壤中的去除过程主要有植物吸收积累、土壤微生物降解和非生物损失.本研究中柳树对PYR的吸收积累总量为土壤中总量的0.11%~0.16%,说明柳树吸收对PYR去除的贡献率较低,这与Lu and Zhu[13]的报道一致.本研究中,土壤PYR的去除率在78.5%~89.7%,说明土壤中芘的去除主要通过土壤微生物降解和非生物损失.Chigbo and Batty [14]在研究柠檬酸促进玉米修复铜⁃芘复合污染土壤时发现柠檬酸的使用能显著提高PYR的去除率.而在我们所研究的柳树根际土壤中,柠檬酸对土壤中PYR的植物吸收起抑制作用.
图3
图3
柠檬酸对柳树富集PYR的影响
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.3
Effects of citric acid on pyrenen bioaccumulation by willow
2.2 柠檬酸对土壤Cd和PYR的影响
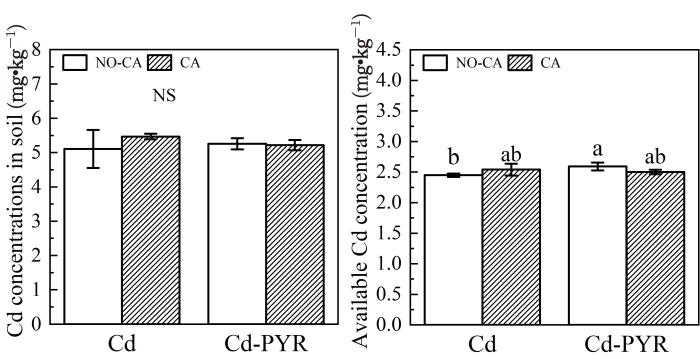
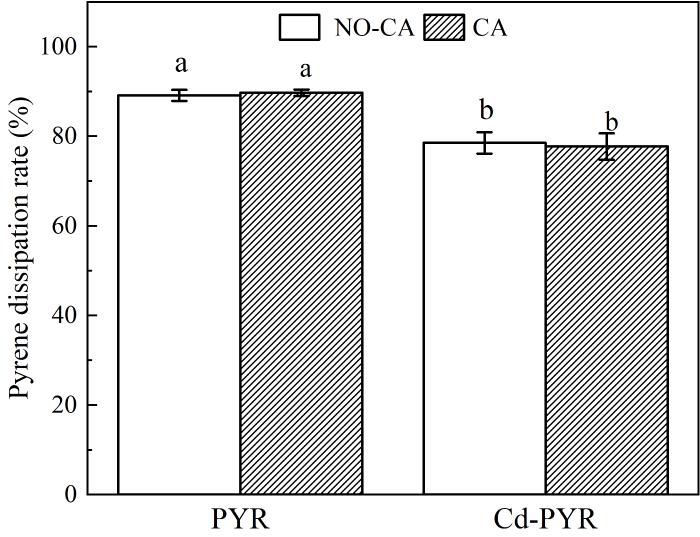
在Cd单一和Cd⁃PYR复合污染组中,添加柠檬酸没有对土壤中Cd浓度和有效态Cd含量产生显著影响(图4).在不添加柠檬酸处理组中,与单一Cd污染相比,Cd⁃PYR复合污染处理组中Cd有效态浓度显著提高,说明PYR通过直接或间接的方式影响了土壤中Cd的形态.添加柠檬酸后,与单一Cd污染相比,Cd⁃PYR复合污染中有效态Cd变化不显著,说明柠檬酸缓解了PYR对Cd形态的影响.图5显示土壤中PYR浓度为1.62~3.39 mg·kg-1,显著低于初始土壤中的PYR浓度(15 mg·kg-1),Cd的存在对PYR的去除产生显著抑制;在PYR单一和复合污染组中,柠檬酸对PYR的去除没有显著影响(去除率分别降低10.4%和11.8%).
图4
图4
柠檬酸对土壤Cd浓度和有效态Cd浓度的影响
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.4
Effects of citric acid on Cd concentrations and available Cd concentrations in soil
图5
图5
土壤中PYR的去除率
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.5
Pyrene disspation rates in different treatments after 60 d
植物吸收污染物的主要限制因素是污染物的生物可利用性,可生物降解的低分子量有机酸被认为具有羧基官能团,能够有效螯合重金属提高重金属的生物可利用性[15],并且有研究报道柠檬酸能够提高重金属(如Cu,Cd,Pb)在土壤中溶解性从而提高植物富集能力[16-17].同时,柠檬酸能提高诸如多环芳烃和有机氯农药等有机污染物的溶解性而提高植物吸收 [18].本研究中,添加柠檬酸并未提高柳树对PYR的吸收和土壤中PYR的去除率,且在复合污染中,柳树对芘的提取有所降低,提取总量显著减少,这可能是由于植物种类和污染物性质差异所致.Agnello et al[19]研究也报道了添加柠檬酸未提高紫花苜蓿对复合污染的植物吸收.本研究中,尽管添加柠檬酸提高了柳树根部对Cd的吸收,但由于添加柠檬酸导致了柳树生物量的降低,从而导致柳树对Cd吸收总量减少.柳树地上部对Cd的转运不仅受根部Cd浓度的影响,还受到柳树自身生理生化过程的影响.金属离子从植物根系转运到地上部组织主要受到两个过程控制:一是从木质部薄壁细胞转载到导管,二是在导管中的运输,后者主要受到根压和蒸腾流的影响[20].此外,由于Cd和PYR共同存在抑制了柳树对Cd的吸收,即使添加柠檬酸,复合污染柳树对Cd的提取总量也比单一Cd污染少了16.9 μg.由于根际环境的复杂性和植物吸收转运Cd的机制并未完全获悉,柠檬酸强化植物吸收污染物的机理有待进一步研究考证.
2.3 柠檬酸对柳树生长的影响
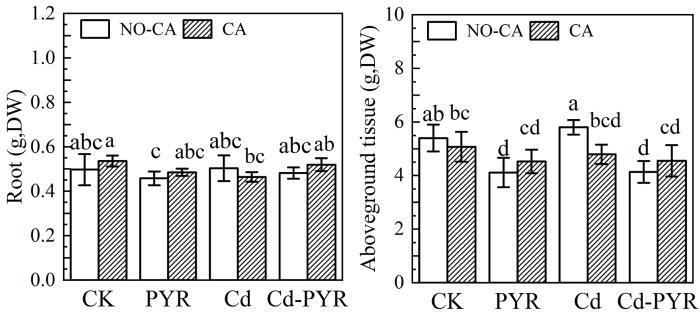
经过60 d实验,添加柠檬酸处理组和未添加处理组柳树均正常生长,外观无明显受毒害症状.CK组中,柠檬酸对柳树根部和地上部生物量无显著影响,Cd污染处理组中,柠檬酸显著抑制柳树地上部的生长(17.4%)(图6).与CK组相比,Cd和PYR单一或复合污染对柳树根部生物量没有显著影响,但PYR污染和Cd⁃PYR复合污染显著抑制了柳树地上部的生物量(分别降低23.8%和23.4%),而添加柠檬酸后则缓解了这种抑制作用.PYR为典型持久性有机污染物,对植物有较强的氧化损伤作用,Wang et al[21]研究发现暴露于10 mg·kg-1 PYR的Kandelia obovata,生物量显著下降27.62%,暴露于Cd⁃PYR复合污染时生物量下降16.28%.本研究中柠檬酸加入导致PYR在柳树中的富集显著降低,这可能也导致PYR对柳树的毒性降低,柳树的生长抑制得到缓解,生物量没有再产生显著下降.
图6
图6
柳树地上部和根部的生物量干重
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.6
Dry weight of root and aboveground biomass of willows
2.4 柠檬酸对柳树体内矿质元素含量的影响
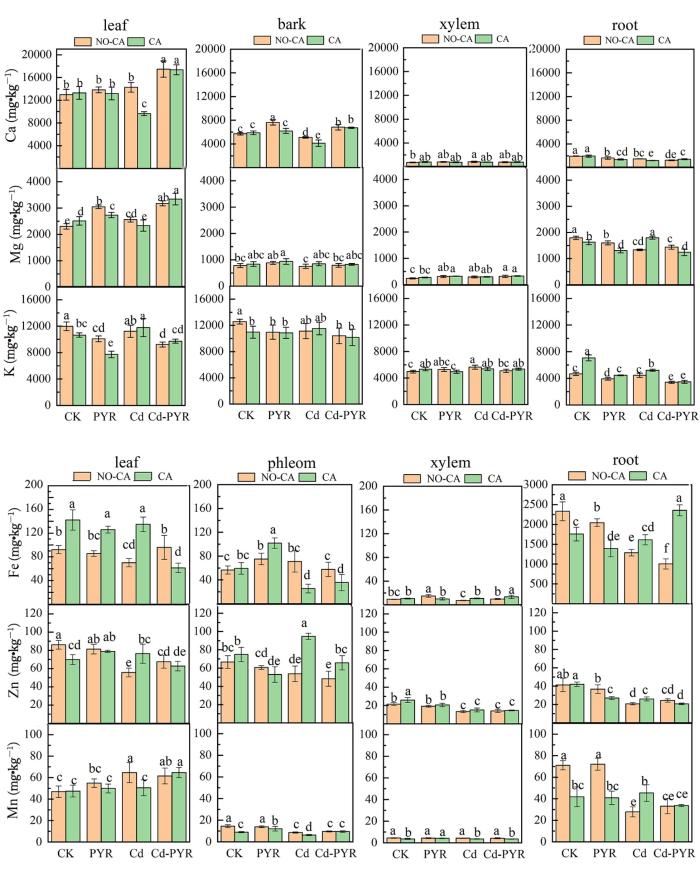
矿质元素对植物的生长发育十分重要,图7列出了Ca,Mg,K,Fe,Mn,Zn在柳树不同部位(根部、木质部、皮、叶片)的浓度对比.由图可知添加柠檬酸降低了柳树叶片中Ca,Mg,K,Mn含量,但提高了叶片Fe含量.柳树皮部必需元素Fe和Zn的分布受到柠檬酸影响较大,在单一Cd污染处理组中,添加柠檬酸使柳树皮部Zn浓度升高了77.4%.柠檬酸对柳树木质部矿质元素的分布影响较小,其影响趋势因元素的不同而有所差异.在柳树根部,矿质元素Fe和Mn浓度受到柠檬酸的显著影响,在单一PYR土壤中,矿质元素Fe和Mn的浓度分别减低了32.0%和43.0%,在Cd⁃PYR复合污染下,Fe浓度则升高了134.5%,Mn的差异不显著.
图7
图7
柠檬酸对柳树不同部位营养元素的影响
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.7
Effects of citric acid on nutrient elements in different tissues of willow
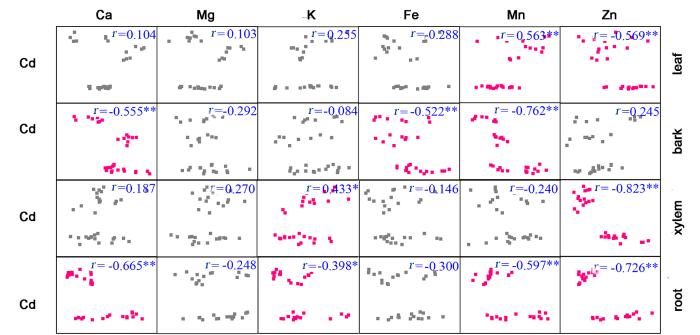
对柳树各部位的矿质元素与Cd的分布进行Pearson相关性分析发现,柳树根部、皮部、叶片的Cd浓度与Zn和Fe浓度存在极显著负相关(图8),说明柳树对Cd的吸收转运与锌的吸收转运存在拮抗效应;柳树皮和根中Cd的浓度与元素Ca,Fe,K,Mn的浓度也存在显著负相关,说明重金属Cd影响了柳树对矿质元素的吸收,对柳树产生了负面影响.
图8
图8
柳树体内元素Cd,Ca,Mg,K,Fe,Mn,Zn相关性分析
Correlationcoefficients significant at p<0.05 are indicated with *,p<0.01 are indicated with ** , Pearson correlation coefficients (r) are shown at the top of individual cell
Fig.8
Scatter plots of concentrations of Cd,Ca,Mg,K,Fe,Mn and Zn in willows
2.5 柠檬酸对柳树叶片光合作用的影响
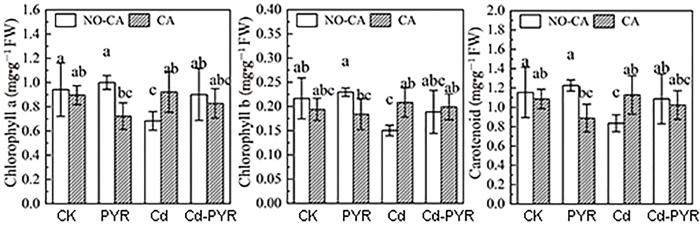
Cd、PYR单一和复合污染各处理组柳树叶片中叶绿素a、叶绿素b和类胡萝卜素如图9所示.在单一PYR污染土壤中,添加柠檬酸使柳树叶片中叶绿素a、叶绿素b和类胡萝卜素分别降低了27.8%,19.9%和27.6%,而在单一Cd污染土壤中,柠檬酸使柳树叶片中叶绿素a、叶绿素b和类胡萝卜素分别提高了35.1%,38.5%和35.0%,在CK和Cd⁃PYR复合污染土壤中,柠檬酸对光合色素含量没有显著影响.
图9
图9
柠檬酸对柳树叶片中色素的影响
n=4,不同字母表示显著差异,p<0.05,NO⁃CA表示未添加柠檬酸组;CA表示添加柠檬酸组
Fig.9
Effects of citric acid on photosynthetic pigments in leaves of willow
添加柠檬酸对柳树的净光合作用速率(Pn)没有显著影响(表2),但对单一Cd污染和Cd⁃PYR复合污染处理组柳树叶片的气孔导度(gs)和细胞间CO2浓度(Ci)产生显著影响.在单一Cd污染处理组中,添加柠檬酸使柳树叶片的gs显著提高了33.7%,在Cd⁃PYR复合污染处理组中,添加柠檬酸使柳树叶片的gs和Ci分别显著提高了56.8%和13.9%.
表2 柠檬酸对柳树叶片气体交换参数的影响
Table 2
| Treatment | Pn | gs | Ci | |
|---|---|---|---|---|
| µmol·m⁻²·s⁻¹ | (mol·m⁻²·s⁻¹) | µmol·mol⁻¹ | ||
| NO⁃CA | CK | 7.03 ± 1.20b | 0.12 ± 0.03bc | 291.5 ± 7.93ab |
| PYR | 8.66 ± 0.97ab | 0.14 ± 0.01abc | 280.1 ± 15.83abc | |
| Cd | 7.92 ± 1.65ab | 0.12 ± 0.01c | 272.8 ± 15.51bc | |
| Cd⁃PYR | 8.10 ± 0.91ab | 0.11 ± 0.12c | 262.4 ± 9.94c | |
| CA | CK | 8.94 ± 1.15ab | 0.16 ± 0.02ab | 290.2 ± 12.4ab |
| PYR | 9.91 ± 2.12a | 0.17 ± 0.05a | 285.3 ± 16.4ab | |
| Cd | 8.78 ± 1.97ab | 0.15 ± 0.02ab | 291.7 ± 22.1ab | |
| Cd⁃PYR | 8.94 ± 1.79ab | 0.17 ± 0.03a | 298.9 ± 6.00a | |
表3 柠檬酸对柳树叶片荧光参数的影响
Table 3
| Treatment | Fv/Fm | ΦPSⅡ | qP | |
|---|---|---|---|---|
| NO⁃CA | CK | 0.776±0.018a | 0.119±0.020b | 0.280±0.063c |
| PYR | 0.781±0.015a | 0.154±0.083ab | 0.314±0.155bc | |
| Cd | 0.774±0.006a | 0.126±0.024ab | 0.322±0.054bc | |
| Cd⁃PYR | 0.793±0.010a | 0.116±0.034b | 0.253±0.078c | |
| CA | CK | 0.782±0.015a | 0.177±0.015a | 0.403±0.037ab |
| PYR | 0.783±0.020a | 0.199±0.029a | 0.443±0.048a | |
| Cd | 0.778±0.016a | 0.179±0.028a | 0.399±0.032ab | |
| Cd⁃PYR | 0.782±0.019a | 0.185±0.032a | 0.414±0.045ab | |
光合作用是植物生长发育的物质和能量来源,已有研究表明Cd会降低光合作用强度[23],而光合作用中心系统Ⅱ是植物逆境下敏感脆弱的部位[24],通过对柳树光合作用和营养元素进行综合分析,能够阐明柳树在Cd胁迫下的耐性和柠檬酸影响植物生长的可能机理.研究表明,Cd胁迫影响植物叶片中光合色素分子的合成[25],本实验中,单一Cd污染处理组中柳树叶片中叶绿素a、叶绿素b和类胡萝卜素含量也显著降低,表现出相同的抑制作用,但是柠檬酸的添加缓解了这种抑制作用.进一步分析柳树的气体交换参数与叶绿素荧光参数,发现Cd污染没有影响柳树的净光合作用速率和叶绿素荧光参数.Fv/Fm是研究PSⅡ反应中心利用所捕获激发能情况的重要指标[26],可以直观的表示植物在逆境情况下受胁迫的程度.本实验中所有处理组的Fv/Fm均接近0.8,说明柠檬酸添加未使柳树的光合系统受到较大胁迫.但添加柠檬酸使柳树叶片的qP有所升高,说明此时柳树可能通过能量耗散机制来适应柠檬酸的影响.
3 结 论
柠檬酸对土壤中Cd有效态含量和PYR浓度的影响不显著,Cd单一污染中,添加柠檬酸虽然刺激了柳树根部对Cd的吸收,但抑制了柳树地上各组织的生物量,使柳树对Cd的提取总量和转运系数分别减少了11.0%和12.0%,表明单一Cd污染土壤中添加柠檬酸不能有效提高柳树对Cd的提取效率;而Cd⁃PYR复合污染中,添加柠檬酸提高了柳树叶、皮中的Cd浓度和地上部生物量,使Cd的总提取量显著提高19.5%,PYR的富集量下降了35%,PYR的植物富集只占总量的0.16%,表明复合污染下添加柠檬酸能够提高柳树对Cd的提取效率.在单一和复合Cd污染处理组中,添加柠檬酸促进了柳树叶片中色素的合成,增加了柳树叶片光合作用参数.
参考文献
Nitrogen combined with biochar changed the feedback mechanism between soil nitrification and Cd availability in an acidic soil
Effects of heavy metals and chelants on phytoremediation capacity and on rhizobacterial communities of maize
Biochar immobilizes soil⁃borne arsenic but not cationic metals in the presence of low⁃molecular⁃weight organic acids
Comparison of synthetic chelators and low molecular weight organic acids in enhancing phytoextraction of heavy metals by two ecotypes of Sedum alfredii Hance
Citric acid assisted phytoremediation of cadmium by Brassica napus L
EDTA、柠檬酸对Cd、Ni污染土壤植物修复的影响
Effects of EDTA and citric acid on phytoremediation of Cd and Ni contaminated Soil
Plant uptake and enhanced dissipation of di (2⁃ethylhexyl) phthalate (DEHP) in spiked soils by different plant species
苏丹草对土壤中菲芘的修复作用
The remediation of phenanthrene and pyrene in soil by sudan grass (Sorghum vulgare L
.).
Polynuclear aromatic hydrocarbons (PAHs) mediate cadmium toxicity to an emergent wetland species
柳树对镉⁃芘复合污染土壤的修复潜力与耐受性研究
Interaction effects on uptake and toxicity of cadmium and pyrene in willows from co⁃contaminated soil
Reducing plant uptake of PAHs by cationic surfactant⁃enhanced soil retention
Chelate⁃assisted phytoremediation of Cu⁃pyrene⁃contaminated soil using Z
Organic acids on the growth,anatomical structure,biochemical parameters and heavy metal accumulation of Iris lactea var
Comparison of natural organic acids and synthetic chelates at enhancing phytoextraction of metals from a multi⁃metal contaminated soil
Effect of short⁃chain organic acids and pH on the behaviors of pyrene in soil–water system
Citric acid⁃ and Tween® 80⁃assisted phytoremediation of a co⁃contaminated soil:Alfalfa (Medicago sativa L
.)
Interactive effects of cadmium and pyrene on contaminant removal from co⁃contaminated sediment planted with mangrove Kandelia obovata (S
L.)
Chlorophyll fluorescence:A probe of photosynthesis in vivo
Changes of photosynthetic activities of maize (Zea mays L
.)
碱性盐胁迫对桑树幼苗叶片叶绿素荧光和激发能分配的影响
Effects of chlorophyll fluorescence characteristics and energy allocation pathways in leaves of mulberry seedlings under alkali salt stress
植物镉忍耐的分子机理
Molecular mechanisms of plant resistance to cadmium toxicity
镉胁迫对水稻光合、叶绿素荧光特性和能量分配的影响
Effects of cadmium stress on photosynthesis,chlorophyll fluorescence characteristics and excitation energy distribution in leaves of rice