Surface and interface chemistry of clay minerals
1
2007
... 粘土矿物广泛分布于土壤、沉积物和地层等,因其粒度小、含量高、分布广而发挥着重要的地球化学作用,其中蒙脱石是地表、近地表最常见的2∶1型粘土矿物,对重金属和有机污染物有很好的吸附效果[1].蒙脱石八面体层和四面体层中心离子通常被低价态离子取代而使粘土片层整体带负电荷,因而粘土层间往往存在一定量的Na+,Ca2+等离子平衡结构层电荷;由于蒙脱石层间局域的相对开放性,层间阳离子容易和溶液中的阳离子发生交换[2].这一晶体化学特征使粘土矿物具有遇水膨胀性和离子交换性等特点,阳离子交换容量远高于伊利石和高岭石等粘土矿物[3],因为后者一般只有表面断键位置的离子参与交换.蒙脱石对重金属离子和部分有机物的固定也通过阳离子交换完成,因此,研究蒙脱石的阳离子交换过程有助于理解粘土矿物⁃流体相互作用和重金属污染修复能力. ...
Cation?exchange kinetics on montmorillonite using pressure?jump relaxation
1
1993
... 粘土矿物广泛分布于土壤、沉积物和地层等,因其粒度小、含量高、分布广而发挥着重要的地球化学作用,其中蒙脱石是地表、近地表最常见的2∶1型粘土矿物,对重金属和有机污染物有很好的吸附效果[1].蒙脱石八面体层和四面体层中心离子通常被低价态离子取代而使粘土片层整体带负电荷,因而粘土层间往往存在一定量的Na+,Ca2+等离子平衡结构层电荷;由于蒙脱石层间局域的相对开放性,层间阳离子容易和溶液中的阳离子发生交换[2].这一晶体化学特征使粘土矿物具有遇水膨胀性和离子交换性等特点,阳离子交换容量远高于伊利石和高岭石等粘土矿物[3],因为后者一般只有表面断键位置的离子参与交换.蒙脱石对重金属离子和部分有机物的固定也通过阳离子交换完成,因此,研究蒙脱石的阳离子交换过程有助于理解粘土矿物⁃流体相互作用和重金属污染修复能力. ...
不同粘土矿物对赖氨酸的吸附行为对比研究
1
2018
... 粘土矿物广泛分布于土壤、沉积物和地层等,因其粒度小、含量高、分布广而发挥着重要的地球化学作用,其中蒙脱石是地表、近地表最常见的2∶1型粘土矿物,对重金属和有机污染物有很好的吸附效果[1].蒙脱石八面体层和四面体层中心离子通常被低价态离子取代而使粘土片层整体带负电荷,因而粘土层间往往存在一定量的Na+,Ca2+等离子平衡结构层电荷;由于蒙脱石层间局域的相对开放性,层间阳离子容易和溶液中的阳离子发生交换[2].这一晶体化学特征使粘土矿物具有遇水膨胀性和离子交换性等特点,阳离子交换容量远高于伊利石和高岭石等粘土矿物[3],因为后者一般只有表面断键位置的离子参与交换.蒙脱石对重金属离子和部分有机物的固定也通过阳离子交换完成,因此,研究蒙脱石的阳离子交换过程有助于理解粘土矿物⁃流体相互作用和重金属污染修复能力. ...
不同粘土矿物对赖氨酸的吸附行为对比研究
1
2018
... 粘土矿物广泛分布于土壤、沉积物和地层等,因其粒度小、含量高、分布广而发挥着重要的地球化学作用,其中蒙脱石是地表、近地表最常见的2∶1型粘土矿物,对重金属和有机污染物有很好的吸附效果[1].蒙脱石八面体层和四面体层中心离子通常被低价态离子取代而使粘土片层整体带负电荷,因而粘土层间往往存在一定量的Na+,Ca2+等离子平衡结构层电荷;由于蒙脱石层间局域的相对开放性,层间阳离子容易和溶液中的阳离子发生交换[2].这一晶体化学特征使粘土矿物具有遇水膨胀性和离子交换性等特点,阳离子交换容量远高于伊利石和高岭石等粘土矿物[3],因为后者一般只有表面断键位置的离子参与交换.蒙脱石对重金属离子和部分有机物的固定也通过阳离子交换完成,因此,研究蒙脱石的阳离子交换过程有助于理解粘土矿物⁃流体相互作用和重金属污染修复能力. ...
On the power of soils to absorb manure
1
1850
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Base exchange equilibria in clays
1
1933
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Equilibria of the base?exchange reactions of bentonites,permutites,soil colloids,and zeolites
1
1932
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Adsorption studies on clay minerals
1
1953
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Ueber basenaustausch an permutiten
1
1927
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Hysteresis in the binary exchange of cations on 2:1 clay minerals:a critical review
1
1994
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Cation exchange equilibria on clay minerals
1
1952
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Extended version of gouy?chapman electrostatic theory as applied to the exchange behavior of clay in natural waters
1
1983
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Alkali cation selectivity and fixation by clay minerals
1
1980
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Highly selective ion exchanger in clay minerals and zeolites
1
1986
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Relationship between cation exchange selectivity and crystalline swelling in expanding 2:1 phyllosilicates
1
1997
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Structure of water adsorbed on a mica surface
1
2002
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Computer simulation of interlayer molecular structure in sodium montmorillonite hydrates
1
1995
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
Monte carlo simulations of wyoming sodium montmorillonite hydrates
2
2001
... 蒙脱石的阳离子交换性能很早就受到关注.Way[4]最早发现土壤在吸收溶液中K+离子的同时会释放出等电荷量的Ca2+和Mg2+离子;Marshall and Gupta[5]率先提出粘土矿物晶体结构与阳离子交换密切相关;随后一系列研究用化学热力学理论描述蒙脱石阳离子交换过程并预测不同粘土矿物的阳离子交换容量[6,7].通过在溶液中增加不同浓度乙醇,Wiegner and Jenny[8]较早证明了粘土矿物对金属离子的选择性吸附与金属离子的水化能力有关.阳离子交换过程在热力学上为可逆过程,但水化能力差异较大的阳离子间的交换往往会有滞后效应[9],属于动力学效应.Eriksson[10]和Neal and Cooper[11]曾尝试用双扩散层模型解释阳离子交换机制,但这一模型显然只能描述蒙脱石外表面的过程而无法揭示过于狭窄的层间过程.Eberl[12]计算了包括静电作用和水化能的阳离子交换自由能,认为金属离子水化状态是影响阳离子可交换性的主要因素.与此同时,蒙脱石阳离子交换还受控于层间水含量和环境溶液组成以及环境温度等因素[13,14].近年来迅速发展的分子模拟技术可以有效揭示粘土矿物⁃流体相互作用的微观机制,得到了粘土矿物层间局域结构的精细特征[15,16]和层间离子的活动性[17]. ...
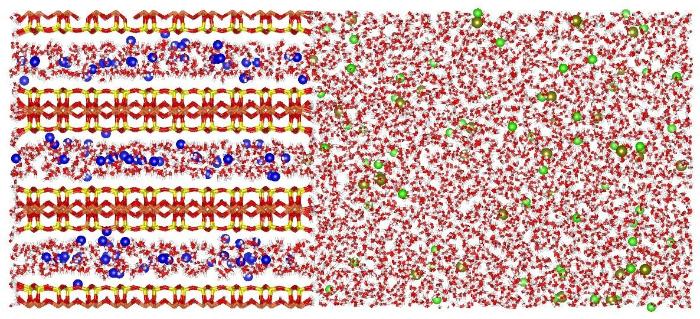
... 本研究采用怀俄明型蒙脱石(化学式:Na0.75[Si7.75Al0.25][Al3.5Mg0.5]O20(OH)4)[17].蒙脱石相由10×5×3个单胞组成,其(010)边缘面与含盐流体接触(图1).蒙脱石边缘面的Al和Si均联接羟基,结构层内的类质同像取代位置随机分布并避免发生在相邻中心原子对或者边缘面上[18,19].蒙脱石层间离子均为Na+离子,层间水量按钠基蒙脱石比较稳定的两层层间水的量设定[20].孔隙流体的体积略大于粘土模型,阳离子分别为K+,Ca2+,Mg2+,Ba2+等金属离子,利用常见的Cl-离子平衡电荷,为了有利于达到阳离子交换平衡,设定了较高的流体盐浓度0.7 mol·L-1.在计算模拟中该模型设定为三维周期性边界. ...
The distribution of aluminum in the tetrahedra of silicates and aluminates
1
1954
... 本研究采用怀俄明型蒙脱石(化学式:Na0.75[Si7.75Al0.25][Al3.5Mg0.5]O20(OH)4)[17].蒙脱石相由10×5×3个单胞组成,其(010)边缘面与含盐流体接触(图1).蒙脱石边缘面的Al和Si均联接羟基,结构层内的类质同像取代位置随机分布并避免发生在相邻中心原子对或者边缘面上[18,19].蒙脱石层间离子均为Na+离子,层间水量按钠基蒙脱石比较稳定的两层层间水的量设定[20].孔隙流体的体积略大于粘土模型,阳离子分别为K+,Ca2+,Mg2+,Ba2+等金属离子,利用常见的Cl-离子平衡电荷,为了有利于达到阳离子交换平衡,设定了较高的流体盐浓度0.7 mol·L-1.在计算模拟中该模型设定为三维周期性边界. ...
Molecular dynamics simulations of anion exclusion in clay interlayer nanopores
1
2016
... 本研究采用怀俄明型蒙脱石(化学式:Na0.75[Si7.75Al0.25][Al3.5Mg0.5]O20(OH)4)[17].蒙脱石相由10×5×3个单胞组成,其(010)边缘面与含盐流体接触(图1).蒙脱石边缘面的Al和Si均联接羟基,结构层内的类质同像取代位置随机分布并避免发生在相邻中心原子对或者边缘面上[18,19].蒙脱石层间离子均为Na+离子,层间水量按钠基蒙脱石比较稳定的两层层间水的量设定[20].孔隙流体的体积略大于粘土模型,阳离子分别为K+,Ca2+,Mg2+,Ba2+等金属离子,利用常见的Cl-离子平衡电荷,为了有利于达到阳离子交换平衡,设定了较高的流体盐浓度0.7 mol·L-1.在计算模拟中该模型设定为三维周期性边界. ...
Changes in the interlayer structure and thermodynamics of hydrated montmorillonite under basin conditions:molecular simulation approaches
1
2016
... 本研究采用怀俄明型蒙脱石(化学式:Na0.75[Si7.75Al0.25][Al3.5Mg0.5]O20(OH)4)[17].蒙脱石相由10×5×3个单胞组成,其(010)边缘面与含盐流体接触(图1).蒙脱石边缘面的Al和Si均联接羟基,结构层内的类质同像取代位置随机分布并避免发生在相邻中心原子对或者边缘面上[18,19].蒙脱石层间离子均为Na+离子,层间水量按钠基蒙脱石比较稳定的两层层间水的量设定[20].孔隙流体的体积略大于粘土模型,阳离子分别为K+,Ca2+,Mg2+,Ba2+等金属离子,利用常见的Cl-离子平衡电荷,为了有利于达到阳离子交换平衡,设定了较高的流体盐浓度0.7 mol·L-1.在计算模拟中该模型设定为三维周期性边界. ...
Fast parallel algorithms for short?range molecular dynamics
1
1995
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
Molecular models of hydroxide,oxyhydroxide,and clay phases and the development of a general force field
1
2004
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
Structure of hydrated gibbsite and brucite edge surfaces:DFT results and further development of the clayff classical force field with metal–O–H angle bending terms
1
2017
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
Interaction models for water in relation to protein hydration
1
1981
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
Numerical integration of the cartesian equations of motion of a system with constraints:molecular dynamics of n?alkanes
1
1977
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
Effects of temperature on the measured cation?exchange capacities of ando soils
1
1971
... 计算模拟所用软件包为Lammps[21],原子间作用力主要包含库仑力和范德华力.参考前人计算模拟研究,用Clayff[22]和Clayff⁃modify[23]力场描述蒙脱石及其边缘面,水分子使用SPC(Simple⁃Point⁃Charge)模型[24],各离子用点电荷表示.初始溶液结构随机生成,每个溶液相都先在正则系综(NVT)下平衡3.0 ns再与蒙脱石通过(010)面接触,最终体系大小为51.8 Å×100 Å×46.5 Å.然后将整个体系在恒温恒压系综(NPT)下再模拟30~40 ns并达到平衡,随后用2.0 ns的NVT系统来统计数据.所有模拟时间步长都是1 fs,水分子通过SHAKE算法[25]约束.前人研究表明温度对阳离子交换的选择性影响不大[26],并且为避免高温下有的物相发生溶解,模拟体系处于室温条件下(298 K,1.01×105 Pa),并使用三维周期性边界. ...
蒙脱石对赖氨酸和壳聚糖的吸附实验研究
1
2014
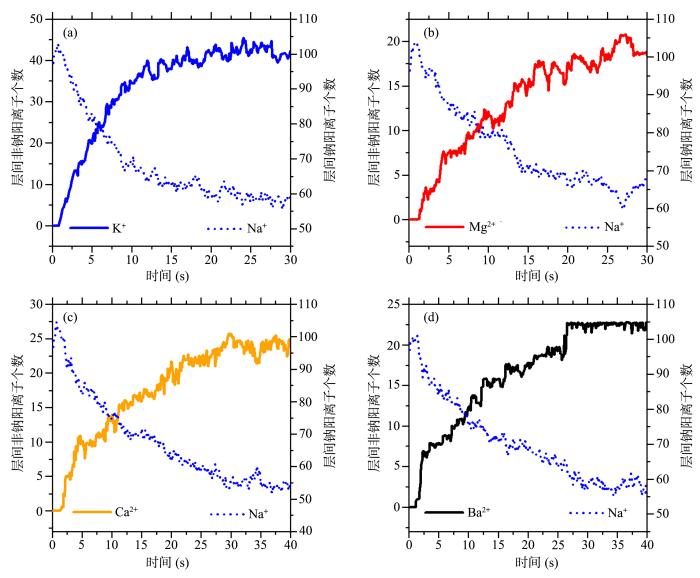
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
蒙脱石对赖氨酸和壳聚糖的吸附实验研究
1
2014
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
Influence of montmorillonite tactoid size on Na?Ca cation exchange reactions
1
2011
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
Effects of ph and ionic strength on the cation exchange capacity of soils with variable charge
1
1981
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
Adsorption of barium(II) on montmorillonite:an exafs study
1
2001
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
Charge density and Na?K?Ca exchange on smectites
1
1987
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
Potassium selectivity in certain montmorillonitic soil clays
2
1972
... 分子模拟揭示了蒙脱石层间阳离子交换的过程,可用阳离子类型和含量随时间的变化表达(图2).在模拟达到平衡前,蒙脱石层间Na+离子含量不断降低,来自溶液的阳离子(K+,Ca2+,Mg2+,Ba2+)逐渐升高并逐渐达到最大值,即阳离子交换达到平衡.结果显示,K+(图2a)的阳离子交换体系在20 ns内即可达到平衡;Mg2+离子(图2b)的最慢,30 ns后还存在明显的波动;Ca2+(图2c)和Ba2+(图2d)交换Na+离子的速度略慢,需要25 ns才可达到平衡.达到交换平衡的蒙脱石层间仍存在一定数量的Na+离子.取达到交换平衡后10 ns内的层间阳离子交换量的统计平均值来代表阳离子交换量,分别为:K+(289.1 mmolNa·100 g-1),Mg2+(254.2 mmolNa·100 g-1),Ca2+(328.0 mmolNa·100g-1),Ba2+(308.4 mmolNa·100 g-1).计算所得的蒙脱石阳离子交换量明显高于一些实验报道(如:94.5 mmolNa·100 g-1)[27],主要是因为模拟所用的蒙脱石模型具有相对高的层电荷和孔隙溶液的离子浓度明显偏高[28,29].从统计结果看,在二价阳离子中Ca2+离子的交换量最高,Ba2+离子次之,Mg2+离子交换量最低.事实上,孔隙流体中的金属离子不仅进入蒙脱石层间,在粘土边缘面上也可能与阳离子形成内球络合[30].在本文模拟中观察到了Ba2+离子与蒙脱石八面体层发生内球络合,若将之计入,钡离子总体交换量可达353.7 mmolNa·100 g-1.需要说明的是,由于本文模拟的粘土矿物尺寸较小,金属阳离子与粘土表面络合作用较弱,数十纳秒内没有观察到表面内球络合只代表表面络合作用较弱.总的看来,二价阳离子进入钠基蒙脱石层间数量的顺序为:Ba2+>Ca2+>Mg2+,即水化能力弱的阳离子倾向于交换更多的Na+离子.K+离子的交换过程较快,但交换量却相对较低,这与前人的实验结果一致[31,32]. ...
... 其中L为蒙脱石层间部分或者溶液部分在y方向上的宽度,中n为正整数,的定义同前文相关函数中的定义.计算得到的自扩散系数与前人类似模拟的结果一致[37,38],阳离子在蒙脱石层间扩散显著慢于溶液中(表1).对于二价阳离子而言,Ba2+离子的扩散速率最低,Mg2+的扩散速率最高,Ca2+离子居于中间,这一顺序和三种离子的水化能力从弱到强恰好一致;但Ca2+在粘土层间的扩散系数比溶液条件的下降最多,结构层对Mg2+的影响相对最小,可能与水合离子的尺寸有关;由于层间存在两种金属离子,二者之间可能也存在复杂的相互影响[39].结构层对K+离子的抑制效果最明显,这可能与K+离子更容易靠近蒙脱石表面并与表面六元环络合有关[32]. ...
A thermodynamic understanding of clay?swelling inhibition by potassium ions
1
2006
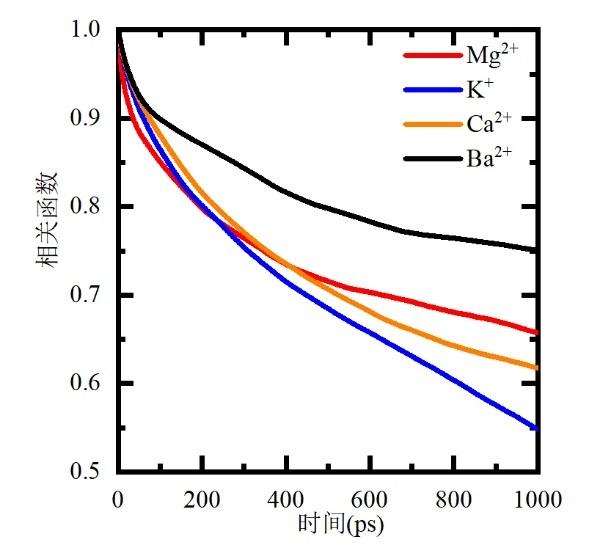
... 若在时刻t阳离子在蒙脱石层间,则h(t)=1,否则h(t)=0,当且仅当在0到t这段时间内阳离子均在蒙脱石层间时SC(t)=1.四种阳离子在蒙脱石层间的自相关函数(图3)显示,Ba2+离子的相关函数随时间减小得最慢,即两层水蒙脱石吸持Ba2+离子的能力最好.Mg2+离子相关函数在开始很小一段时间内下降很快,但需要更长的时间达到平衡,模拟动态图像显示Mg2+离子跨越蒙脱石边缘完全进入层间较难.从图3还可以看出蒙脱石对Ca2+离子的固定能力较弱,会与孔隙流体有频繁的交换.鉴于K+离子作为层间补偿离子时倾向于形成一层层间水的蒙脱石水合状态[33],在Na+和K+共存于层间时层间水量会有所下降,进而层间距减小,但在本文模拟研究中固定了层间距,这会导致计算得到的K+离子活动性比真实情况显著偏高,故在此不讨论K+的活动性. ...
Diffusion?driven transport in clayrock formations
1
2012
... 阳离子交换的速度主要由其扩散速率决定[34,35],基于分子动力学模拟结果可计算各离子沿离子交换方向(y方向)的扩散系数,用于对比不同于阳离子的交换速度.因受蒙脱石结构层的限制,阳离子在层间域内和溶液中的自扩散系数显著不同,为此把整个体系划分为蒙脱石层间和溶液相两部分分别求离子的扩散系数.具体的扩散系数可通过式(2)计算得到[36]: ...
Rate?limited cation exchange in thin bentonitic barrier layers
1
2006
... 阳离子交换的速度主要由其扩散速率决定[34,35],基于分子动力学模拟结果可计算各离子沿离子交换方向(y方向)的扩散系数,用于对比不同于阳离子的交换速度.因受蒙脱石结构层的限制,阳离子在层间域内和溶液中的自扩散系数显著不同,为此把整个体系划分为蒙脱石层间和溶液相两部分分别求离子的扩散系数.具体的扩散系数可通过式(2)计算得到[36]: ...
On the calculation of diffusion coefficients in confined fluids and interfaces with an application to the liquid?vapor interface of water
1
2004
... 阳离子交换的速度主要由其扩散速率决定[34,35],基于分子动力学模拟结果可计算各离子沿离子交换方向(y方向)的扩散系数,用于对比不同于阳离子的交换速度.因受蒙脱石结构层的限制,阳离子在层间域内和溶液中的自扩散系数显著不同,为此把整个体系划分为蒙脱石层间和溶液相两部分分别求离子的扩散系数.具体的扩散系数可通过式(2)计算得到[36]: ...
Molecular dynamics simulation of diffusion and electrical conductivity in montmorillonite interlayers
1
2016
... 其中L为蒙脱石层间部分或者溶液部分在y方向上的宽度,中n为正整数,的定义同前文相关函数中的定义.计算得到的自扩散系数与前人类似模拟的结果一致[37,38],阳离子在蒙脱石层间扩散显著慢于溶液中(表1).对于二价阳离子而言,Ba2+离子的扩散速率最低,Mg2+的扩散速率最高,Ca2+离子居于中间,这一顺序和三种离子的水化能力从弱到强恰好一致;但Ca2+在粘土层间的扩散系数比溶液条件的下降最多,结构层对Mg2+的影响相对最小,可能与水合离子的尺寸有关;由于层间存在两种金属离子,二者之间可能也存在复杂的相互影响[39].结构层对K+离子的抑制效果最明显,这可能与K+离子更容易靠近蒙脱石表面并与表面六元环络合有关[32]. ...
Water and ions in clays:unraveling the interlayer/micropore exchange using molecular dynamics
2
2007
... 其中L为蒙脱石层间部分或者溶液部分在y方向上的宽度,中n为正整数,的定义同前文相关函数中的定义.计算得到的自扩散系数与前人类似模拟的结果一致[37,38],阳离子在蒙脱石层间扩散显著慢于溶液中(表1).对于二价阳离子而言,Ba2+离子的扩散速率最低,Mg2+的扩散速率最高,Ca2+离子居于中间,这一顺序和三种离子的水化能力从弱到强恰好一致;但Ca2+在粘土层间的扩散系数比溶液条件的下降最多,结构层对Mg2+的影响相对最小,可能与水合离子的尺寸有关;由于层间存在两种金属离子,二者之间可能也存在复杂的相互影响[39].结构层对K+离子的抑制效果最明显,这可能与K+离子更容易靠近蒙脱石表面并与表面六元环络合有关[32]. ...
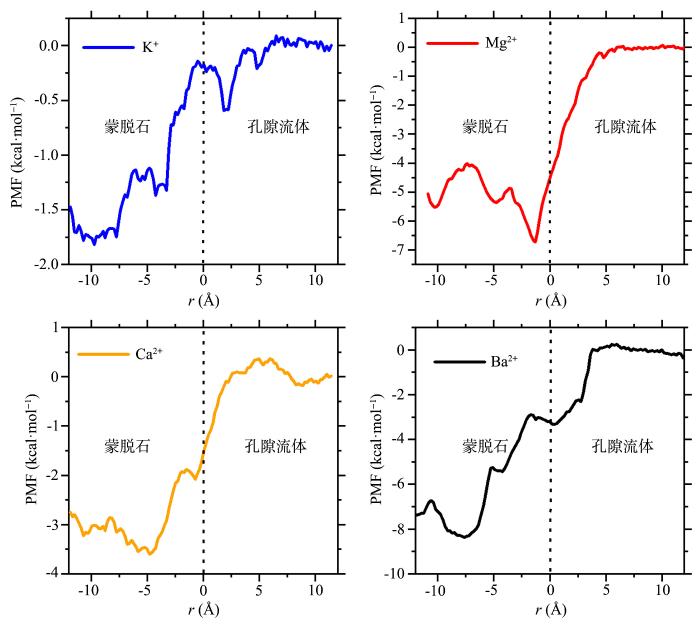
... 热力学积分方法可以计算蒙脱石层间和溶液相间阳离子交换自由能[40,41],选择合适的反应路径计算平均力势的方法可以获得单个阳离子从溶液进入粘土层间的能量变化[38].本文以y轴为反应坐标,采用伞形采样[42]方法计算,得到了不同阳离子进入蒙脱石层间的自由能变化情况(图5).结果表明:蒙脱石层间的金属阳离子能量比在溶液中更低;四种离子中Ba2+离子释出的能量最大(K+:1.500.33 kcal·mol-1,Ca2+:3.250.40 kcal·mol-1,Mg2+:4.720.62 kcal·mol-1,Ba:7.401.18 kcal·mol-1),所以Ba2+离子更容易停留在蒙脱石层间;Mg2+离子进出蒙脱石层间时完全被水化,受蒙脱石表面影响较小,所以Mg2+离子的自由能曲线最平滑.Mg2+离子在进入蒙脱石层间时存在能量最低点(-1.0 Å处),自相关函数显示的Mg2+离子频繁进出层间的现象可能与之有关. ...
Hydration and mobility of interlayer ions of (Nax,Cay)?montmorillonite:a molecular dynamics study
1
2014
... 其中L为蒙脱石层间部分或者溶液部分在y方向上的宽度,中n为正整数,的定义同前文相关函数中的定义.计算得到的自扩散系数与前人类似模拟的结果一致[37,38],阳离子在蒙脱石层间扩散显著慢于溶液中(表1).对于二价阳离子而言,Ba2+离子的扩散速率最低,Mg2+的扩散速率最高,Ca2+离子居于中间,这一顺序和三种离子的水化能力从弱到强恰好一致;但Ca2+在粘土层间的扩散系数比溶液条件的下降最多,结构层对Mg2+的影响相对最小,可能与水合离子的尺寸有关;由于层间存在两种金属离子,二者之间可能也存在复杂的相互影响[39].结构层对K+离子的抑制效果最明显,这可能与K+离子更容易靠近蒙脱石表面并与表面六元环络合有关[32]. ...
Hydration energy determines isovalent cation exchange selectivity by clay minerals
2
2006
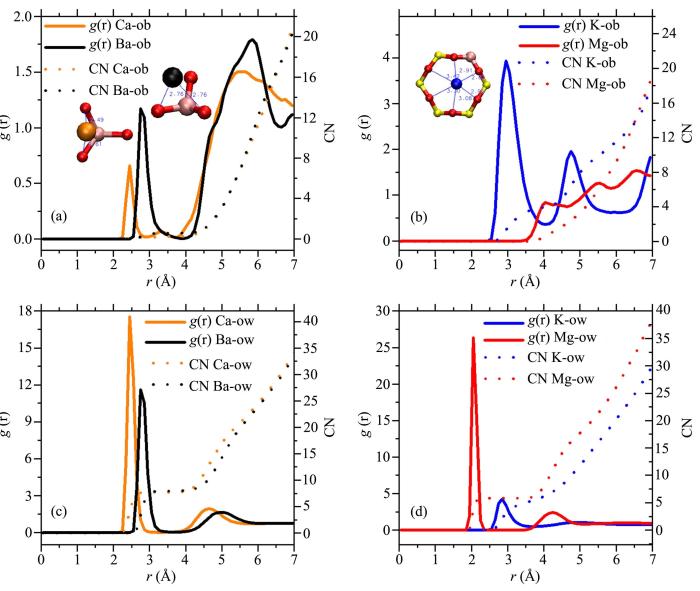
... 其中A是中心原子,B是配位原子,NA⁃B是A原子周围r与r+dr范围内存在的B原子数.由图4a和图4b可以看出Ca2+离子和Ba2+离子第一层络合内存在1~2个粘土表面O原子,K+离子与多个粘土表面O原子络合,但是Mg2+离子只和水分子络合,几乎不和粘土表面存在络合作用.事实上,阳离子与蒙脱石表面的络合作用与其水化能力有关[40],水化能力强的阳离子倾向于与水络合.Ca2+和Ba2+多位于蒙脱石四面体取代位上方(图4a),K+则占据硅氧烷六元环中央(图4b).在阳离子与水中氧的径向分布图中(图4c和图4d),Mg2+离子在2.05 Å处具有尖锐峰,配位数为6;Ca2+和Ba2+离子亦有显著的水合峰,但宽度相对较大,配位数在6~7之间,K+离子的水合峰最弱,配位数在4左右,离子一般被束缚在硅氧烷六元环上方(图4b). ...
... 热力学积分方法可以计算蒙脱石层间和溶液相间阳离子交换自由能[40,41],选择合适的反应路径计算平均力势的方法可以获得单个阳离子从溶液进入粘土层间的能量变化[38].本文以y轴为反应坐标,采用伞形采样[42]方法计算,得到了不同阳离子进入蒙脱石层间的自由能变化情况(图5).结果表明:蒙脱石层间的金属阳离子能量比在溶液中更低;四种离子中Ba2+离子释出的能量最大(K+:1.500.33 kcal·mol-1,Ca2+:3.250.40 kcal·mol-1,Mg2+:4.720.62 kcal·mol-1,Ba:7.401.18 kcal·mol-1),所以Ba2+离子更容易停留在蒙脱石层间;Mg2+离子进出蒙脱石层间时完全被水化,受蒙脱石表面影响较小,所以Mg2+离子的自由能曲线最平滑.Mg2+离子在进入蒙脱石层间时存在能量最低点(-1.0 Å处),自相关函数显示的Mg2+离子频繁进出层间的现象可能与之有关. ...
On the driving force of cation exchange in clays:insights from combined microcalorimetry experiments and molecular simulation
1
2009
... 热力学积分方法可以计算蒙脱石层间和溶液相间阳离子交换自由能[40,41],选择合适的反应路径计算平均力势的方法可以获得单个阳离子从溶液进入粘土层间的能量变化[38].本文以y轴为反应坐标,采用伞形采样[42]方法计算,得到了不同阳离子进入蒙脱石层间的自由能变化情况(图5).结果表明:蒙脱石层间的金属阳离子能量比在溶液中更低;四种离子中Ba2+离子释出的能量最大(K+:1.500.33 kcal·mol-1,Ca2+:3.250.40 kcal·mol-1,Mg2+:4.720.62 kcal·mol-1,Ba:7.401.18 kcal·mol-1),所以Ba2+离子更容易停留在蒙脱石层间;Mg2+离子进出蒙脱石层间时完全被水化,受蒙脱石表面影响较小,所以Mg2+离子的自由能曲线最平滑.Mg2+离子在进入蒙脱石层间时存在能量最低点(-1.0 Å处),自相关函数显示的Mg2+离子频繁进出层间的现象可能与之有关. ...
Nonphysical sampling distributions in monte carlo free?energy estimation:Umbrella sampling
1
1977
... 热力学积分方法可以计算蒙脱石层间和溶液相间阳离子交换自由能[40,41],选择合适的反应路径计算平均力势的方法可以获得单个阳离子从溶液进入粘土层间的能量变化[38].本文以y轴为反应坐标,采用伞形采样[42]方法计算,得到了不同阳离子进入蒙脱石层间的自由能变化情况(图5).结果表明:蒙脱石层间的金属阳离子能量比在溶液中更低;四种离子中Ba2+离子释出的能量最大(K+:1.500.33 kcal·mol-1,Ca2+:3.250.40 kcal·mol-1,Mg2+:4.720.62 kcal·mol-1,Ba:7.401.18 kcal·mol-1),所以Ba2+离子更容易停留在蒙脱石层间;Mg2+离子进出蒙脱石层间时完全被水化,受蒙脱石表面影响较小,所以Mg2+离子的自由能曲线最平滑.Mg2+离子在进入蒙脱石层间时存在能量最低点(-1.0 Å处),自相关函数显示的Mg2+离子频繁进出层间的现象可能与之有关. ...