环氧化合物是一种非常有价值的基础化合物,是有机合成的重要中间体,由于有活泼的环氧基存在,可与多种物质反应生成具高附加值的化合物.环氧环己烷广泛地用于农药克螨特、环氧树脂的活性稀释剂和添加剂、光敏涂料和可降解塑料等[1].
目前,环氧环己烷的工业生产方法主要有两种:一是从轻质油(在环己烷氧化制备环己酮、环己醇的工艺过程中会产生一种轻馏分,其中含有30% wt左右的环氧环己烷)中分离得到,由于轻质油的成分比较复杂,难以得到高纯度的环氧环己烷.二是化学合成法,空气环氧化法、过氧化物环氧化法、氯醇法是传统的合成方法.氯醇法、过氧酸法对设备腐蚀严重,反应工艺复杂,而空气环氧化法一般只适用于低级烯烃[2].过氧化氢环氧化法是一种绿色环保、具有应用潜力的方法,以杂多化合物做催化剂、双氧水做氧源催化烯烃环氧化已有很广泛的研究[3,4,5,6,7,8,9].Venturello et al[10,11],Matoba et al[12]和Ishii et al[13]分别发展了具有相似结构的基于杂多酸盐的催化体系.其中Venturello et al[10,11]研究了在相转移条件下[PW4O24]3-杂多酸催化H2O2环氧化环己烯,反应体系需添加缓冲剂调节水溶液的pH,抑制环氧环己烷的水解.O2是理想的氧化剂,绿色廉价.Xi et al[14,15]将可循环使用的2⁃乙基蒽氢醌(EAHQ)用作还原剂,以分子氧为氧化剂、杂多酸盐为催化剂催化环氧化多种烯烃.该反应中2⁃乙基蒽氢醌氧化生成2⁃乙基蒽醌,2⁃乙基蒽醌加氢再生成2⁃乙基蒽氢醌,实际反应中H2O2起到氧化剂的作用,产物为环氧化合物和H2O.本文以环己烯为底物、杂多酸盐为催化剂、H2O2为氧化剂,研究了该反应的工艺条件并进行了优化,在此基础上,将反应扩大10倍与100倍进行验证.
1 实验部分
1.1 试剂与仪器
环己烯(AR,≥99.5%)、30%过氧化氢(AR)、氯仿(AR,≥99.5%)、二氯甲烷(AR,≥99.5%)、四氯化碳(AR,≥99.5%)、1,2⁃二氯乙烷(AR,≥99.5%)、1,1,2⁃三氯乙烷(AR,≥99.5%)、四氢呋喃(AR,≥99.5%)、甲苯(AR,≥99.5%)、盐酸(AR,36%)、氯化十六烷基吡啶(CP,≥99.0%)、十六烷基三甲基溴化铵(AR,≥99.0%)、三乙基苄基溴化铵(AR,≥99.0%)、氯化钾(AR,≥99.5%)、苯基磷酸二钠(AR,≥99.0%),均购自国药集团化学试剂有限公司,氯化钠(AR,≥99.5%)、碳酸钠(AR,≥99.8%)、磷酸氢二钠(AR,≥99.8%)、磷酸二氢钠(AR,≥99.8%)、磷酸二氢钾(AR,≥99.5%)、氯化铵(AR,≥99.8%)、硫酸钠(AR,≥99.8%),均购自上海凌峰化学试剂有限公司.
1.2 催化剂的制备
1.2.1 催化剂[Q+]3[PW4O163-]的制备
[Q+]3[PW4O163-]的制备参考文献[16].称取3.3 g Na2WO4·2H2O (0.01 mol),加入10 mL去离子水,充分搅拌溶解,向钨酸钠溶液中滴加36% wt盐酸溶液2.03 g得钨酸悬浊液,向钨酸悬浊液中加入7 mL 30% H2O2,60 ℃搅拌至无色得过氧钨酸溶液,冷至室温后加入85% wt H3PO4溶液0.29 g (W∶P=4∶1),搅拌30 min,再向该溶液中滴加2.69 g氯化十六烷基吡啶的50 mL二氯甲烷溶液,搅拌反应30 min,静置分层,取有机相在40 ℃减压蒸馏,得淡黄色固体,在40 ℃下真空干燥2 h即得反应控制相转移催化剂[C5H5NC16H33]3[PO4(WO3)4](PTC1).
催化剂[(CH3)3NC16H33]3[PO4(WO3)4](PTC2)和[C6H5CH2N(C2H5)3]3[PO4 (WO3)4](PTC3)的制备方法同上.
1.2.2 催化剂[C5H5NC16H33]2{[PO3(OH)][WO(O2)2]2}(PTC4)的制备
[C5H5NC16H33]2{[PO3(OH)][WO(O2)2]2}的制备参考文献[17].过氧钨酸溶液制备方法同前.向过氧钨酸溶液中加入1.79 g Na2HPO4·12H2O (5.0 mmol)的5 mL水溶液,搅拌5 min,再向该溶液中滴加3.58 g氯化十六烷基吡啶的10 mL 95%乙醇溶液,搅拌反应1 h,抽滤,分别用水、乙醇、乙醚洗涤数次,在40 ℃下真空干燥2 h即得反应控制相转移催化剂[C5H5NC16H33]2{[PO3(OH)][WO(O2)2]2}.
1.2.3 催化剂[C5H5NC16H33]3{(PO4)[WO(O2)2]2[WO(O2)2(H2O)]}(PTC5)的制备
[C5H5NC16 H33]3{(PO4)[WO(O2)2]2[WO(O2)2(H2O)]}的制备参考文献[17].过氧钨酸溶液制备方法同前.向过氧钨酸溶液中加入0.52 g NaH2PO4·2H2O (3.33 mmol)的5 mL水溶液,搅拌5 min,后续步骤同前.
1.2.4 催化剂[C5H5NC16H33]2{(PhPO4)[WO(O2)2]2(PTC6)}的制备
[C5H5NC16H33]2{(PhPO4)[WO(O2)2]}的制备参考文献[18].过氧钨酸溶液的制备方法同前.称取1.09g Na2PhPO4·2H2O (0.005 mol)溶于5 mL水,加稀盐酸调pH=2,与过氧钨酸水溶液混合,搅拌10 min,后续步骤同前.
1.3 环氧化反应
小试反应在50 mL的玻璃三口瓶中进行,依次加入催化剂、溶剂、环己烯和双氧水,于设定温度的水浴上回流搅拌,定时取样进行气相色谱(Gas Chromatography,GC)分析.扩大10倍反应在500 mL的玻璃四口瓶中进行,因双氧水用量较大,为防止反应放热太快温度失控,双氧水采用恒压滴液漏斗恒定流量滴加.扩大100倍反应在5 L装有冷凝管和温度计的夹套玻璃反应釜中进行,双氧水也采用恒压滴液漏斗恒定流量滴加.
反应结束后,静置分层,取有机相离心使催化剂沉淀,回收催化剂用甲苯洗涤数次,40 ℃下真空干燥.
1.4 催化剂的表征
NICOLET公司NEXUS870型傅里叶变换红外光谱仪,光谱范围400~4000 cm-1,KBr压片.
1.5 分析方法
岛津GC⁃2014C色谱仪.色谱柱为HP⁃5毛细管柱(30 m×0.32 mm×0.25 μm),FID检测器,载气N2,程序升温:60 ℃
1 min,60~140 ℃ 15 ℃∙min-1 2 min,气化室温度290 ℃,检测器温度295 ℃,进样量0.5 μL,由面积归一法进行定量分析.
2 结果与讨论
2.1 催化剂的表征
图1
图1
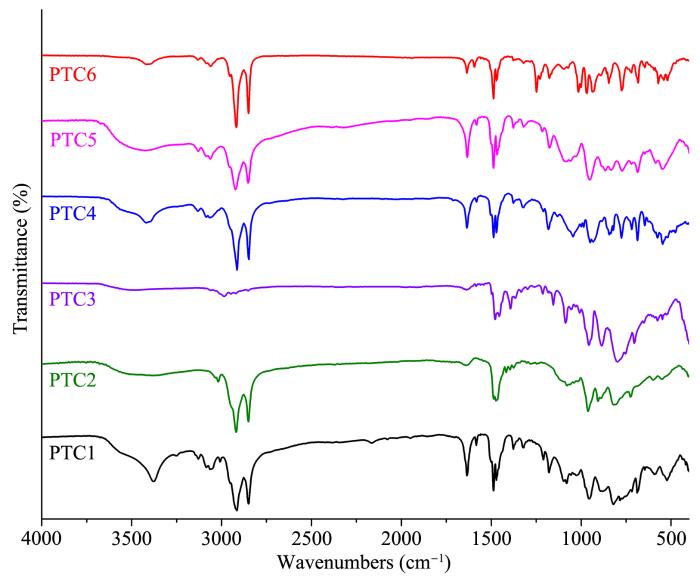
催化剂的红外光谱图
Fig.1
FT⁃IR spectra of catalysts
PTC1:[C5H5NC16H33]3[PO4(WO3)4]
PTC2:[(CH3)3NC16H33]3[PO4(WO3)4]
PTC3:[C6H5CH2N(C2H5)3]3[PO4(WO3)4]
PTC4:[C5H5NC16H33]2{[PO3(OH)][WO(O2)2]2}
PTC5:[C5H5NC16H33]3{(PO4)[WO(O2)2]2[WO (O2)2(H2O)]}
PTC6:[C5H5NC16H33]2{(PhPO4)[WO(O2)2]2}
2.2 反应温度的影响
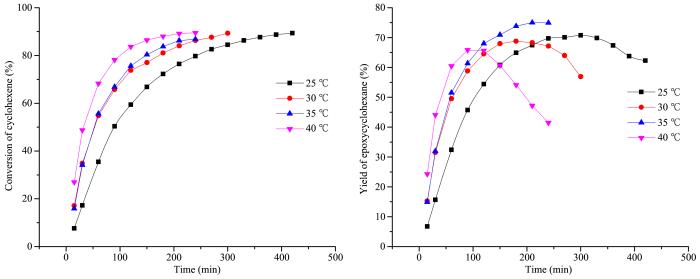
不同的温度对环己烯环氧化的影响如图2所示.可以看到,随着反应温度的增加,反应速度会增加,最终环己烯的转化率都在90%左右.温度越高,环氧环己烷越易水解,选择性越低.当反应温度为35 ℃时,环氧环己烷的产率达到最高的76%.因此综合考虑反应温度在35 ℃较为合适.
图2
图2
不同温度对环己烯环氧化的影响
Fig.2
Effect of temperature on the epoxidation of cyclohexene
solvent:chloroform 15 mL,CH 0.1 mol,n (CH)∶n (H2O2)=1∶1,
catalyst:0.84 g (PTC1=0.43 [n (catalyst)∶n (CH)]),KCl 0.032 g
2.3 不同溶剂的影响
不同溶剂对环己烯环氧化的影响如表1所示.
表1 不同溶剂对环己烯环氧化的影响
Table 1
| Entry | Solvent | Conversion(%) | Yield (%) |
|---|---|---|---|
| 1 | Dichloromethane | 80.45 | 67.32 |
| 2 | Chloroform | 80.66 | 73.28 |
| 3 | Carbon tetrachloride | 12.33 | 10.30 |
| 4 | 1,2⁃Dichloroethane | 34.72 | 31.92 |
| 5 | Trichloroethane | 62.37 | 55.72 |
| 6 | Tetrahydrofuran | 18.67 | 17.21 |
| 7 | Toluene | 29.88 | 18.86 |
溶液的性质在催化环己烯环氧化的过程中起很重要的作用.从表1可以看出,在极性氯代溶剂二氯甲烷、氯仿和三氯乙烷中,环己烯的转化率都较高;在非极性溶剂四氯化碳、1,2⁃二氯乙烷、甲苯中,环己烯的转化率都较低;在极性溶剂四氢呋喃中,环己烯的转化率较低.综合考虑环己烯的转化率和环氧环己烷的收率,氯仿是较为合适的溶剂.
2.4 不同添加剂的影响
不同的添加剂对环己烯环氧化的影响如表2所示.
表2 不同添加剂对环己烯环氧化的影响
Table 2
| Entry | Additives | Conversion(%) | Yield(%) |
|---|---|---|---|
| 1 | None | 70.2 | 7.54 |
| 2 | NaCl | 71.5 | 53.8 |
| 3 | Na2CO3 | 59.1 | 58.2 |
| 4 | Na2HPO4 | 86.2 | 68.3 |
| 5 | NaH2PO4 | 84.1 | 48.9 |
| 6 | KH2PO4 | 83.5 | 52.1 |
| 7 | KCl | 86.9 | 82.0 |
| 8 | NH4Cl | 35.1 | 34.5 |
| 9 | Na2SO4 | 79.5 | 50.1 |
1∶1,catalyst:0.84 g (PTC1),T:35 ℃,additives:0.041 g,
reaction time:3 h
以双氧水作为氧源催化环己烯环氧化的副产物是H2O2,随着反应的进行,H2O2的量也在增加,环氧环己烷在酸性条件下与H2O2接触易水解生成环己二醇.在高溶剂用量的情况下(v (CHCl3)∶v (H2O2)≈30∶1),有机相体积远大于水相,环氧环己烷与H2O2的接触少,不易水解,但在实际工业化生产中,如此高的溶剂用量是不切实际的.如表2所示,在v (CHCl3)∶
v (H2O2)≈3∶1时,不加任何的添加剂,环己烯的转化率为70.2%,而环氧环己烷的收率仅为7.54%,为了提高环氧环己烷的选择性,需要添加适当的添加剂抑制环氧环己烷的水解.从表2可以看出,Na2HPO4,NaH2PO4等缓冲试剂可以降低反应体系的酸性,NaCl,KCl等盐可以降低环氧环己烷在水相中的溶解度,从而抑制环氧环己烷的水解.综合考虑环己烯的转化率和环氧环己烷的收率,KCl是较合适的添加剂.
2.5 不同添加剂用量的影响
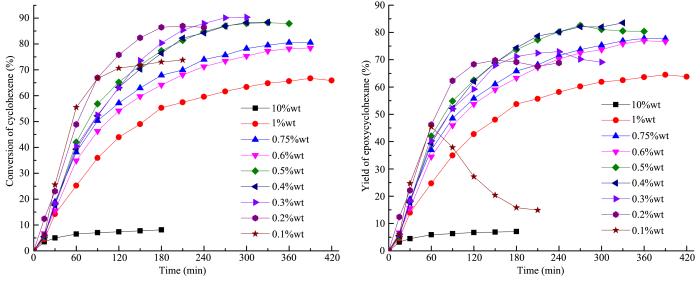
不同添加剂用量对环己烯环氧化的影响如图3所示.随着KCl用量的增加,环己烯的转化率呈下降趋势,环氧环己烷的选择性呈上升趋势,综合考虑环己烯的转化率和环氧环己烷的收率,较为合适的添加剂用量是0.4% wt~0.5% wt of CH.
图3
图3
不同添加剂用量对环己烯环氧化的影响
Fig.3
Effect of additive loading on epoxidation of cyclohexene
solvent:CHCl3 30 mL,CH 0.1 mol,n (CH)∶n (H2O2)=1∶1,catalyst:0.84 g (PTC1),T:35 ℃,additives:KCl (%wt of CH)
2.6 不同催化剂用量的影响
不同催化剂用量对环己烯环氧化的影响如表3所示.
表3 不同催化剂用量对环己烯环氧化的影响
Table3
| Entry | Catalyst loading(%mol of CH) | Conversion(%) | Yield (%) |
|---|---|---|---|
| 1 | 0.05 | 10.86 | 10.05 |
| 2 | 0.25 | 53.64 | 6.54 |
| 3 | 0.43 | 70.11 | 7.54 |
| 4 | 0.5 | 74.20 | 18.26 |
| 5 | 0.75 | 75.50 | 31.82 |
1∶1,catalyst:PTC1,T:35 ℃,reaction time:3 h
从表3可以看出,催化剂用量对环己烯的转化率以及环氧环己烷的选择性都有显著的影响,随着催化剂用量的增加,环己烯的转化率和环氧环己烷的选择性也会相应增加.
2.7 不同溶剂用量的影响
不同溶剂用量对环己烯环氧化的影响如表4所示.
表4 不同溶剂用量对环己烯环氧化的影响
Table 4
| Entry | Solvent loading (mL) | Conversion(%) | Yield (%) |
|---|---|---|---|
| 1 | 7.5 | 72.4 | 3.25 |
| 2 | 10 | 82.2 | 32.8 |
| 3 | 15 | 86.8 | 74.5 |
| 4 | 20 | 90.9 | 77.3 |
| 5 | 30 | 87.0 | 81.8 |
1∶1,catalyst:0.84 g (PTC1),T:35 ℃,additive:0.032 g (KCl),
reaction time:3 h
从表4可以看出,溶剂用量对环氧环己烷的选择性有显著的影响,随着氯仿用量的增加,环氧环己烷的选择性也会增加,考虑在保持较高的转化率和收率的前提下,尽可能地降低溶剂的量,15 mL是较为合适的溶剂用量.
2.8 不同催化剂的影响
不同催化剂对环己烯环氧化的影响如表5所示.
表5 不同催化剂对环己烯环氧化的影响
Table 5
| Entry | Catalyst | Conversion(%) | Yield(%) |
|---|---|---|---|
| 1 | PTC1 | 91.83 | 3.70 |
| 2 | PTC2 | 25.93 | 23.03 |
| 3 | PTC3 | 0.79 | 0.59 |
| 4 | PTC4 | 92.10 | 78.15 |
| 5 | PTC5 | 74.63 | 0.851 |
| 6 | PTC6 | 72.83 | 1.93 |
1∶1,catalyst:0.43 [n (catalyst)∶n (CH)],T:35 ℃,reaction time:6 h
从表5可以看出,催化剂PTC1和PTC4催化的反应环己烯转化率较高,分别为91.83%和92.1%,而PTC4催化剂催化反应的收率还达到了78.15%,在未加添加剂的前提下,PTC4催化剂催化活性最高,选择性最高.
2.9 扩大10倍与100倍实验
基于50 mL的玻璃三口瓶中的小试而优选的工艺条件(催化剂PTC1,用量0.43% mol,反应温度35 ℃,溶剂为氯仿(15 mL),环己烯0.1 mol,n (CH)∶
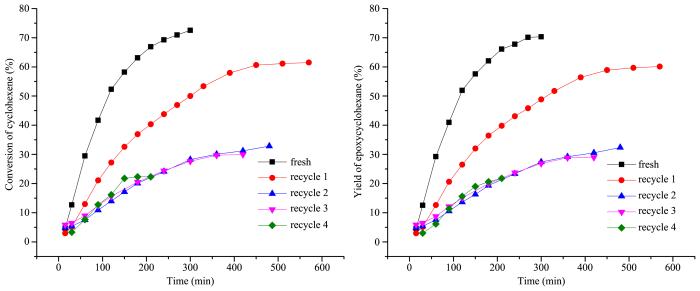
n (H2O2)=1∶1,添加剂为KCl (0.032 g)),将该环氧化反应分别于500 mL的玻璃三口瓶和5 L的玻璃夹套反应釜中放大10倍和100倍进行实验.放大实验与小试实验的对比结果如图4所示.
图4
图4
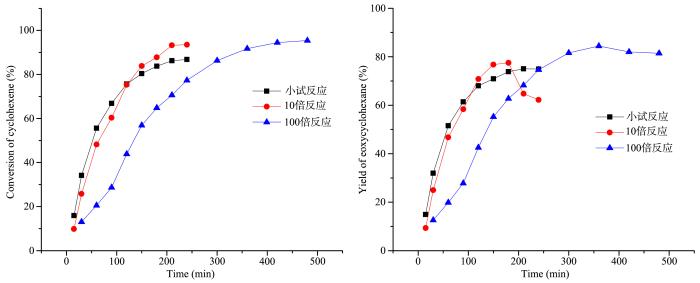
不同规模的反应对环己烯环氧化的影响
Fig.4
Comparison between different⁃sized reactions on the epoxidation of cyclohexene
solvent:CHCl3 15/150/1500 mL,CH 0.1/1/10 mol,n (CH)∶n (H2O2)=1∶1,catalyst:0.84/8.4/84 g,
T:35 ℃,additive:0.032/0.32/3.2 g (KCl),dropping rate of H2O2:0.72 mL·min-1
结果显示,实验放大10倍与100倍后,环己烯转化率与环氧环己烷的收率分别为93.5%,77.5%以及95.4%,84.4%,相对于小试实验,环己烯转化率与环氧环己烷的收率都有所提升,这可能是由H2O2加入方式不同导致的.小试反应中H2O2由于量少故一次性加入反应,而放大10倍、100倍后为避免反应过于剧烈,H2O2由一次性加入改为缓慢滴加的方式,这样一方面相当于增加单位时间的n (CH)∶n (H2O2),促进反应正方向进行,另一方面也减少双氧水由于体系放热导致分解,提高其利用率,所以使环己烯转化率有所提高.此外高浓度的H2O2也会促进副反应的发生,H2O2缓慢滴加提高环氧环己烷选择性与收率.
图4环氧环己烷收率图中,放大10倍反应中180 min环氧环己烷收率达到最高后开始下降,这是由于反应生成的环氧环己烷与体系中的水反应,水解成环己二醇,使其选择性与收率下降.放大100倍反应中从360 min以后同样如此,只是下降幅度平缓.结合环己烯转化率图来看,放大10倍的反应180 min以后环己烯不再转化,所以水解过程会使得环氧环己烷的收率明显下降,而放大100倍的反应360 min以后H2O2未消耗尽,环己烯继续被氧化为环氧环己烷,氧化的同时伴随着环氧环己烷水解的发生,两者共同作用使环氧环己烷的收率下降并不明显.所以控制反应时间对于提高环氧环己烷收率极为重要.
2.10 催化剂回收实验
PTC2,PTC3的催化效果较差,环己烯的转化率较低,故对PTC1,PTC4,PTC5,PTC6进行了催化剂的质量回收实验,结果如表6所示.
表6 不同催化剂的回收率
Table 6
| Entry | Catalyst | Recovery rate (%,m/m) |
|---|---|---|
| 1 | PTC1 | 77.38 |
| 2 | PTC4 | 35.60 |
| 3 | PTC5 | 28.33 |
| 4 | PTC6 | 32.02 |
1∶1,catalyst:0.84 g,T:35 ℃,reaction time:3 h
Recovery process:After reaction,the catalyst was seperated by centrifugation,washed with toluene.
图5
图5
催化剂PTC1回收实验结果
Fig.5
The results of the recycle of the catalyst PTC1
solvent:CHCl3 15 mL,CH 0.1 mol,n (CH)∶n (H2O2)=1∶1,catalyst:0.84 g,T:35 ℃,reaction time:3h,additive:0.032 g (KCl)
Recovery process:after reaction,the catalyst was seperated by centrifugation,washed with toluene,and used in the next reaction without addition of fresh catalyst.
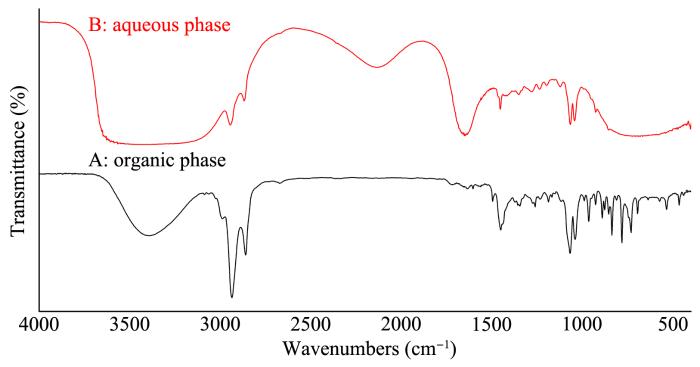
从图5可以看出,随着催化剂PTC1回收次数的增加,环己烯的转化率会逐次降低.从表6中可以看出,催化剂PTC1在催化一次反应后流失了22.62%,理论上反应控制的相转移催化剂在双氧水消耗完毕后会以固体的形式析出,但实验结果显示仍会有一定量的催化剂流失,催化剂的流失意味着下次反应中催化剂量的减少.从表3可以看出,当催化剂用量减少时,环己烯的转化率会下降.在第一次反应结束后,离心分离出催化剂,分别取有机相和水相进行红外表征,红外谱图如图6所示.1024~1125 cm-1的峰属于PO43-的υ(P⁃O)振动,925~960 cm-1的峰属于υ(W=O)振动,892 cm-1附近的峰属于υ(W⁃Ob⁃W)振动,813 cm-1附近的峰属于υ(W⁃Oc⁃W)振动,684~784 cm-1附近的峰属于季铵盐阳离子的振动.水相在1067,1039 cm-1处的吸收峰,有机相在1067,1039,957,927,890,809,778,732,695 cm-1处的吸收峰说明催化剂在水相和有机相中均有残留.
图6
图6
反应结束后水相和有机相的红外光谱图
Fig.6
FT⁃IR spectra of organic phase and aqueous phase after reaction
为了考察催化剂PTC1的重复利用性能,在相同实验条件下取相同质量新鲜催化剂、一次回收以及两次回收的催化剂反应,其中新鲜催化剂的反应进行五组平行反应,以便可以回收到足够的一次回收以及二次回收催化剂.所得结果如表7所示.
表7 催化剂PTC1重复利用实验结果
Table 7
| Entry | Catalyst | Conversion(%) | Yield(%) |
|---|---|---|---|
| 1 | fresh | 86.80 | 74.50 |
| 2 | recycle1 | 87.05 | 74.72 |
| 3 | recycle2 | 86.53 | 74.46 |
1∶1,catalyst:0.84 g,T:35 ℃,reaction time:3 h,additive: 0.032 g (KCl)
Recovery process:after reaction,the catalyst was seperated by centrifugation, washed with toluene,and used in the next reaction without addition of fresh catalyst.
从表7中可以看出二次回收之后环己烯的转化率以及环氧环己烷的收率依旧保持在原来的高度,变化幅度较小,催化剂PTC1重复利用性能较好,唯一存在的问题便是反应结束后难以使催化剂完全析出,催化剂有所损失.
3 总 结
以环己烯为底物,双氧水为氧化剂,杂多酸盐为催化剂,合成环氧环己烷,于50 mL玻璃三口瓶中进行小试,对工艺条件优化.实验结果表明,以PTC1为催化剂,用量0.84 g [0.43% mol (of CH)],反应温度35 ℃,溶剂氯仿(15 mL),环己烯0.1 mol,n (CH)∶n (H2O2)=1∶1,添加剂为KCl (0.032 g),环己烯转化率达到86.8%,环氧环己烷的收率达到74.5%.此外,还考察了不同催化剂的回收效果与实验放大效果,结果表明催化剂在一次反应后均出现了不同程度的流失,其中PTC1的回收率相对较高,但相同质量催化剂的催化效果不变;实验放大10倍与100倍后,环己烯转化率与环氧环己烷的收率分别为93.5%,77.5%以及95.4%,84.4%.
参考文献
环氧环己烷的市场分析及应用前景
Market analysis and application foreground for epoxycyclohexane
环氧环己烷的合成新工艺研究
Novel environment benign process for preparation of cyclohexylene oxide
Polyoxometalate⁃catalysed epoxidation of 1⁃octene with hydrogen peroxide in microemulsions coupled with ultrafiltration
Efficient epoxidation of olefins with ≥99% selectivity and use of hydrogen peroxide
Selective epoxidation of olefins by hydrogen peroxide in water using a polyoxometalate catalyst supported on chemically modified hydrophobic mesoporous silica gel
Solvent⁃anchored supported liquid phase catalysis:polyoxometalate⁃catalyzed oxidations
Homogeneous catalysis by transition metal oxygen anion clusters
Mechanism and dynamics in the H3[PW12O40]⁃catalyzed selective epoxidation of terminal olefins by H2O2
Formation,reactivity,and stability of {PO4[WO(O2)2]4}3-
Heteropolyanions as oxidation catalysts in a 2⁃phases system
A new peroxotungsten heteropoly anion with special oxidizing properties:Synthesis and structure of tetrahexylammonium tetra (diperoxotungsto) phosphate (3⁃)
Quaternary ammonium tetrakis (diperoxotungsto) phosphates (3⁃) as a new class of catalysts for efficient alkene epoxidation with hydrogen peroxide
Epoxidation of allylic alcohols with hydrogen peroxide catalyzed by [PMO12O40]3-[C5H5N+(CH2)15CH3]3
Hydrogen peroxide oxidation catalyzed by heteropoly acids combined with cetylpyridinium chloride
Epoxidation of olefins and allylic alcohols,ketonization of alcohols and diols,and oxidative cleavage of 1,2⁃diols and olefins
Reaction⁃controlled phase⁃transfer catalysis for propylene epoxidation to propylene oxide
Direct epoxidation of olefins catalyzed by heteropoly⁃oxometalates with molecular oxygen and recyclable reductant
Epoxidation of olefins catalyzed by [π⁃C5H5NC16H33]3[PW4O16] with molecular oxygen and a recyclable reductant 2⁃ethylanthrahydroquinone
Studies on polyoxo and polyperoxo⁃metalates part 51:Peroxide⁃catalysed oxidations with heteropoly⁃peroxo⁃tungstates and⁃molybdates
环境友好的丙烯和苯乙烯催化环氧化方法的研究
Studies on environmentally friendly catalytic epoxidation of propylene and styrene
A spectroscopic study on the reaction⁃controlled phase transfer catalyst in the epoxidation of cyclohexene